Коронавирус и другие пандемии.
6,826,860
32,262

Торонто
55 лет
Карма: +264.71
Регистрация: 04.11.2009
Сообщений: 9,034
Читатели: 9
Регистрация: 04.11.2009
Сообщений: 9,034
Читатели: 9
Цитата: Аква от 13.08.2020 21:25:09Все, кто сильно закрывался, и чувствовал себя в шоколаде, получат все, что положено, лишь только приоткроются.
Ага. Помните в Ю. Корее в июне открыли бары и т.д., потом оказалось что один гей, уже больной, посетил 5 баров за одну ночь?
Недавно читал, корейцам пришлось найти и опознать 11,000 человек после этого случая.
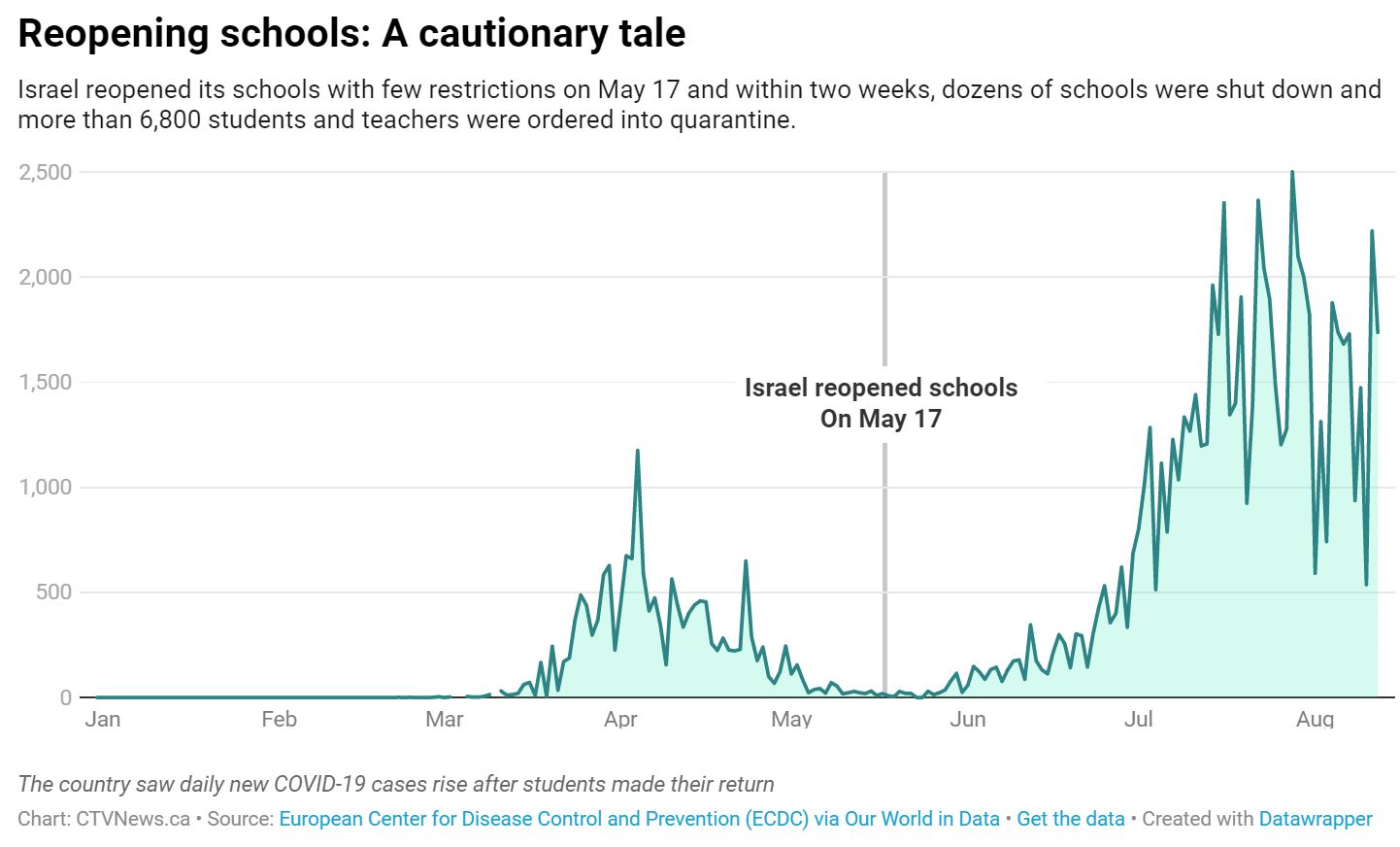
В Израиле в начале мая было всего 23 зараженных в день, они 17 мая загнали детей назад в школы.
В то время была жара, доктора сказали что держите окна открытые в классах для вентиляции, и маски для всех.
https://www.ctvnews.ca/health/…-1.5062834
Результат, в конце июня 240 школ все таки пришлось закрыть, 22,000 учителей и студентов были отправлены в карантин, 2,000 из них были заражены.
.
Карма: +2.83
Регистрация: 25.01.2013
Сообщений: 248
Читатели: 0
Аккаунт заблокирован
Регистрация: 25.01.2013
Сообщений: 248
Читатели: 0
Аккаунт заблокирован
Цитата: Foxhound от 13.08.2020 17:17:28А как было в советские времена?
А в советские времена в основном работали "по-Семашковски", эдакий индустриальный подход в индустриальном обществе. Всех без разбора на зарядку, потом на прививки, потом на обливания, потом строем походить, и потом на субботниках метлой помахать. Ну и конечно хором мыть руки, чистить зубы и закаляться. Плюс - "типовые" нормы питания, правила готовки блюд, "советы поварам и женам" - поменьше сладкого и соленого и о пользе шпината... В принципе - секрет медицины несложен - санитария, закаливание и правильное питание. Это дало значительный рост продолжительности жизни (в царской России продолжительность жизни крестьянина была не более 35 лет, дети умирали до совершеннолетия почти 50%, а в Средней Азии вообще косила холера, тиф, чума - там и до 30ти не дожить). Получилось - что почти вдвое продолжительность выросла - до 50ти лет точно.. А если кто-то будет против - ну вы помните как в тоталитарных обществах борятся с несогласными - таковых не было. Единичные случаи типа аллергии - тоже никого не волновали - "отряд не заметил потери бойца"...
Что касается фармы и лекарств - то есть 2 подхода - "доказательная медицина" и "персонифицированная медицина". Для первой надо длинные клинические исследования с плацебо (простое слепое, двойное слепое и пр) и последующий долгосрочный мониторинг возможных осложнений.. Но надо еще умудриться выйти и на доклинические испытания (примерно из 10 тыс лекарств только ~ 250 доходят до доклинических испытаний по статистике PhRMA) . В итоге этот путь - 10-12 лет, и огромные деньги
Есть например лекарства (онкология в основном) - где на разработку формулы и ее испытания ушло более $1-2 млрд. Само тиражирование лекарств и упаковка - уже копейки..
Для второй - тонкие молекулярные анализы и компьютерное наблюдение. И то и другое дико дорого и долго. И к сожалению, как бы ни говорили не избавлены от "человеческого фактора". Я как физик по первому образованию сильно грустил , видя как безобразно относятся врачи к мат.статистике и обработке результатов лабораторных исследований. Плюс есть и административный фактор - типа тренда с "фуфломицинами", когда под давлением денег или чиновников фармацевты выпускают на рынок лек.средства с абсолютно недоказанной эффективностью. И за немалые деньги.
А жить хочется, поэтому больные сами торопят, рискуют и готовы принимать экспериментальные лекарств . Это уже к персонифицированной медицине и тонкому мониторингу за человеком персонально. В принципе тоже выход - чтобы не ждать бюрократию. (скажем догадывались о пользе лимонов и предотвращении цинги еще во времена Колумба, но прошло почти 200 лет пока это доказал Джеймс Линд в XVIII веке, но в итоге прошло почти 300 лет чтобы эти продукты были включены в обязательный рацион на военных судах и 400 лет - чтобы на гражданских)
Отредактировано: Сергей Д - 14 авг 2020 10:37:29

Карма: +1,898.38
Регистрация: 19.01.2009
Сообщений: 269,300
Читатели: 55
Регистрация: 19.01.2009
Сообщений: 269,300
Читатели: 55
За последние сутки в России выявлено 5 065 новых случаев коронавируса в 83 регионах. Из них 25,9% не имели клинических проявлений болезни.


Зафиксировано 114 летальных исходов. За сутки в России полностью выздоровело 6 568 человек.



Зафиксировано 114 летальных исходов. За сутки в России полностью выздоровело 6 568 человек.

Язык ненависти оказывает сдерживающий эффект на демократический дискурс в онлайн-среде. (c) Еврокомиссия

Санкт-Путинбург
Карма: +56.47
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Цитата: Сергей Д от 14.08.2020 10:35:41В принципе тоже выход - чтобы не ждать бюрократию. (скажем догадывались о пользе лимонов и предотвращении цинги еще во времена Колумба, но прошло почти 200 лет пока это доказал Джеймс Линд в XVIII веке, но в итоге прошло почти 300 лет чтобы эти продукты были включены в обязательный рацион на военных судах и 400 лет - чтобы на гражданских)
Там дело было не в бюрократии, а в экономике. Лимоны были бешенно дорогими в то время. Дешевле было пол-команды списать за борт во время плавания, чем лимонами запасаться. Потом придумали квашеную капусту - и понеслась, Джеймс Кук свои дальние плавания делал уже с очень малыми санитарными потерями.
Эта история (цинга в море) как раз хороша в качестве примера полезности доказательной медицины. Дело в том, что пользу лимонов заметили и оценили быстро, это да. Но, как я уже писал выше - денег они стоили просто бешенных. Поэтому стали изучать, отчего же лимоны такие полезные. Главная гипотеза того времени была простая - лимоны кислые, поэтому дело в кислоте. А раз так - то и другая кислота подойдёт. Что у нас там есть такого, растительного происхождения - уксус? О! Давайте ка поить матросов в плавании уксусом.
И поили уксусом. Пользы для профилактики цинги, понятное дело, в этом не было никакой. Однако моряков массово травили уксусом - очевидно же, что должно помоч! Если бы было бы сделано хоть какое-то подобие клинических испытаний с двойным слепым тестом - было бы очевидно, что уксус ни фига не помогает. Однако - травилим им народ массово, пока не одумались.
Так что доказательная медицина - она не спроста появилась и действительно обоснованная и полезная вещь, позволяющая избежать огромного количества рисков.

Санкт-Путинбург
Карма: +56.47
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Цитата: зарун от 13.08.2020 17:21:24Думаю недолго ждать, когда узнаем об успехов российской вакцины в ликвидации лихорадки Эбола в Гвинее.
Эбола - филовирус. Распространять опыт вакцины против филовирусов на коронавирусы - очень смелое решение. Это если говорить мягко. Это даже не вдаваясь в то, насколько вакцина Гамалеи помогла в Гвинее.
По вакцинам от Эболы - на сегодняшний день, вроде, только rVSV-ZEBOV прошла все фазы испытаний и упоминается ВОЗ как рекомендованная. Все прочие - кандидаты той или иной степени готовности. Наша "гамалейская" как раз вот прямо сейчас завершает клинические испытания на 2000 (две тысячи) добровольцах:
https://clinicaltrials.gov/ct2/show/study/NCT03072030
Особенно хочу заострить внимание на схожести некоторых критериев отбора добровольцев для испытания вакцины Гамалеи от Эболы и Ковида:
ЦитатаInclusion Criteria
- Males and females within the age range from 18 to 60 years;
Exclusion Criteria
- serious thyroid dysfunction or other endocrine disorders (diabetes mellitus) ...
Перевожу:
ЦитатаКритерии отбора
- Мужчины и женщины в возрасте от 18 до 60 лет
В исследовании нельзя принимать участие при наличии
- Серьёзная дисфункция щитовидной железы или другие эндокринные заболевания (сахарный диабет)...
То есть у Гамалеи нет опыта разработки вакцин ни для престарелых, ни для диабетиков. Которые, собственно, и умирают или получают тяжелейшие повреждения лёгких в первую очередь. А 20-30 летним то чего - они только чихают от этого COVIDа, и то в редких случаях, им вакцина и не нужна. Тяжёлые и смертельные случаи там крайне редки.

Москва
51 год
Карма: +344.16
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Цитата: Горец от 14.08.2020 13:46:15Много информационного шума, но НЯП С-5 противопоказана для людей старше 60?
Как бы да, но вчера губернатор московской области анонсировал массовые прививки для пенсионеров.
В принципе, пенсионеров прививать нужно, ибо группа риска. Но не непроверенной же вакциной?
Я своим старикам сказал что в эксперименте им участвовать не нужно.

Москва
37 лет
Карма: +81.62
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Цитата: Доктор Удмурт от 14.08.2020 06:00:47Где Вы на шкале отношения к КОВИД-19 считая от 1 до 10?
1 - Вы надеваете маску, когда едете одни в Вашем автомобиле
10 - Вы близки к раскрытию заговора масонов\n\n
3 - 4: вирус очень опасен, но избегая общественного транспорта, магазинлв и гуляя там гже нет больших скоплений людей (время контакта намного меньше 15 мин) думаю досидеть до вакцинации, причем до момента когда у вакцины будет широкая клиническая практика и не обнаружится явных недостатков.
Отредактировано: Foxhound - 14 авг 2020 14:01:05
А может хватит повторять за западом слово санкции? Ведь реально это "санкции мирового сообщества к виновному" а разрыв части отношений с некоторыми странами!

Санкт-Путинбург
Карма: +56.47
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Цитата: Doctor_D от 14.08.2020 13:53:15Как бы да, но вчера губернатор московской области анонсировал массовые прививки для пенсионеров.
Мне тут другое интересно - а откуда они её в таких количествах возьмут? Для массовой вакцинации. При мощностях на 1.5млн доз в год (оптимистично) - откуда столько возьмётся?
А для массовой вакцинации с целью остановить распространение векторные вакцины в принципе сегодня не годятся - для этого надо штамповать их если не сотнями, то хотя бы десятками миллионов доз в год. Мощностей под это нет. Есть мощности под инактивированные вакцины - например, у "гриппозников". То есть сделав инактивированную вакцину, которую можно выпускать на "гриппозных" мощностях с минимальными их переделками - можно реально остановить эпидемию. Всё равно бОльшую часть года эти мощности простаивают (сезонные штаммы). Такой вакциной, например, является разрабатываемая в ФНЦ Чумакова - поэтому там и возможности её производства в десятки раз выше.

Москва
37 лет
Карма: +81.62
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Цитата: basilevs от 14.08.2020 14:26:00Мне тут другое интересно - а откуда они её в таких количествах возьмут? Для массовой вакцинации. При мощностях на 1.5млн доз в год (оптимистично) - откуда столько возьмётся?
А для массовой вакцинации с целью остановить распространение векторные вакцины в принципе сегодня не годятся - для этого надо штамповать их если не сотнями, то хотя бы десятками миллионов доз в год. Мощностей под это нет. Есть мощности под инактивированные вакцины - например, у "гриппозников". То есть сделав инактивированную вакцину, которую можно выпускать на "гриппозных" мощностях с минимальными их переделками - можно реально остановить эпидемию. Всё равно бОльшую часть года эти мощности простаивают (сезонные штаммы). Такой вакциной, например, является разрабатываемая в ФНЦ Чумакова - поэтому там и возможности её производства в десятки раз выше.
Они заявляют 200 млн до конца года (!) из котоых 30 млн для РФ. Для этого контрактуют мощности сторонних производителей.
Отредактировано: Foxhound - 14 авг 2020 14:43:34
А может хватит повторять за западом слово санкции? Ведь реально это "санкции мирового сообщества к виновному" а разрыв части отношений с некоторыми странами!

Санкт-Путинбург
Карма: +56.47
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Цитата: Foxhound от 14.08.2020 14:43:21Они заявляют 200 млн до конца года (!) из котоых 30 млн для РФ. Для этого контрактуют мощности сторонних производителей.
"Они" - Чумаковцы или Гамалеи? В чумаковцев верю, это примерно соответствует мощностям по производству гриппо-вакцин. В Гамалеи - не верю абсолютно. Таких мощностей просто нет, ни у нас, ни в США, ни в Китае, ни в Европе. Ну разве что сложить вместе все мировые мощности по данному типу вакцин, и то не уверен.
А запускать новые заводы - это месяцы, многие месяцы. Такое оборудование на алибабе не купишь в произвольных количествах.

Москва
51 год
Карма: +344.16
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Не то, чтобы новость (статья в Ланцете от 20 июля 2020).
Речь идет о вакцине на основе аденовирусного вектора.
Хочу обратить внимание на количество добровольцев и дату публикации.
ЦитатаВ китайском исследовании второй фазы приняли участие 508 человек. Исследование было рандомизированным и плацебо-контролируемым: 253 добровольца получили вакцину в одной концентрации, 129 – в другой, еще 126 – пустышку. В статье приводятся данные как о побочных эффектах (ничего смертельного: боль, воспаление, температура, потеря аппетита, головная боль, усталость, тошнота и так далее), так и об эффективности вакцины в сравнении с плацебо (создание Т-клеточного ответа, выработка специфичных антител, выработка интерферона гамма клетками). Несмотря на положительные результаты, авторы лишь делают вывод, что вакцину рекомендуется проверить в следующей – третьей фазе (на большей выборке людей).
Речь идет о вакцине на основе аденовирусного вектора.
Хочу обратить внимание на количество добровольцев и дату публикации.

Москва
37 лет
Карма: +81.62
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Регистрация: 18.02.2011
Сообщений: 13,020
Читатели: 6
Цитата: basilevs от 14.08.2020 15:09:37"Они" - Чумаковцы или Гамалеи? В чумаковцев верю, это примерно соответствует мощностям по производству гриппо-вакцин. В Гамалеи - не верю абсолютно. Таких мощностей просто нет, ни у нас, ни в США, ни в Китае, ни в Европе. Ну разве что сложить вместе все мировые мощности по данному типу вакцин, и то не уверен.
А запускать новые заводы - это месяцы, многие месяцы. Такое оборудование на алибабе не купишь в произвольных количествах.
Они это глава РФПИ и минпромторга. Естественно мощности не только гамалейские. Как я понял управляют процессом там на уровне правительства, а не сами гамалейцы.
Причем мощности для инозаказчиков также ищут зарубежом прямо в странах покупателях.
Отредактировано: Foxhound - 14 авг 2020 16:21:16
А может хватит повторять за западом слово санкции? Ведь реально это "санкции мирового сообщества к виновному" а разрыв части отношений с некоторыми странами!

Санкт-Петербург
Карма: +335.53
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Цитата: basilevs от 14.08.2020 13:32:08Эбола - филовирус. Распространять опыт вакцины против филовирусов на коронавирусы - очень смелое решение. Это если говорить мягко. Это даже не вдаваясь в то, насколько вакцина Гамалеи помогла в Гвинее.
По вакцинам от Эболы - на сегодняшний день, вроде, только rVSV-ZEBOV прошла все фазы испытаний и упоминается ВОЗ как рекомендованная. Все прочие - кандидаты той или иной степени готовности. Наша "гамалейская" как раз вот прямо сейчас завершает клинические испытания на 2000 (две тысячи) добровольцах:
https://clinicaltrials.gov/ct2/show/study/NCT03072030
Особенно хочу заострить внимание на схожести некоторых критериев отбора добровольцев для испытания вакцины Гамалеи от Эболы и Ковида:\n\nПеревожу:\n\nТо есть у Гамалеи нет опыта разработки вакцин ни для престарелых, ни для диабетиков. Которые, собственно, и умирают или получают тяжелейшие повреждения лёгких в первую очередь. А 20-30 летним то чего - они только чихают от этого COVIDа, и то в редких случаях, им вакцина и не нужна. Тяжёлые и смертельные случаи там крайне редки.
Векторные вакцины с использованием различных вирусов - обычная практика в современном фармпроизводстве.
Платформа - это как автомобиль, в котором можно разместить S - белок или какой -то другой оболочечный белок запускающий иммунный ответ, как в данном случае с Эбола и COVID-19.
О том, что пострегистрационные испытания вакцины ГамЭвак-Комби НИИ им. Гамалея в Гвинее закончились, я писал в своём предыдущем посту
Англо-американская вакцина против Эбола - rVSV-ZEBOV хотя и получила разрешение на профилактическое применение среди населения ДРК в очаге лихорадки Эбола, но эффективность её оказалась низкой, о чём говорит высокая смертность среди вакцинированных
пациентов - более 20%. Поэтому рано петь дифирамбы по амерской вакцине.
В составе ФГБУ НИЦЭМ им. Гамалеи входит такое подразделение как НИИ им. Ивановского, в котором работали известнейшие академики и создали отечественных вакцин такие как Чумаков, Тимаков, Смородинцев и др., которые развивали отечественную школу
вакцинопрофилактики, и вопросы особенностей вакцинации престарелых и хронически больных они естественно предусматривали.
Отредактировано: зарун - 14 авг 2020 18:29:06
De die in diem verba volant, scripta manent - изо дня в день слова исчезают, написанное остаётся

Москва
51 год
Карма: +344.16
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Цитата: зарун от 14.08.2020 18:25:17Векторные вакцины с использованием различных вирусов - обычная практика в современном фармпроизводстве.
Платформа - это как автомобиль, в котором можно разместить S - белок или какой -то другой оболочечный белок запускающий иммунный ответ, как в данном случае с Эбола и COVID-19.
О том, что пострегистрационные испытания вакцины ГамЭвак-Комби НИИ им. Гамалея в Гвинее закончились, я писал в своём предыдущем посту
Англо-американская вакцина против Эбола - rVSV-ZEBOV хотя и получила разрешение на профилактическое применение среди населения ДРК в очаге лихорадки Эбола, но эффективность её оказалась низкой, о чём говорит высокая смертность среди вакцинированных
пациентов - более 20%. Поэтому рано петь дифирамбы по амерской вакцине.
В составе ФГБУ НИЦЭМ им. Гамалеи входит такое подразделение как НИИ им. Ивановского, в котором работали известнейшие академики и создали отечественных вакцин такие как Чумаков, Тимаков, Смородинцев и др., которые развивали отечественную школу
вакцинопрофилактики, и вопросы особенностей вакцинации престарелых и хронически больных они естественно предусматривали.
Вообще, разумеется, никакое сходство в "автомобилях", нигде не служит основанием для того, чтобы не проводить клинические исследования. Простите, даже при регистрации дженерика, имеющего не похожий, а *идентичный* состав, проводят исследования биоэквиваоентности (аналог третьей фазы).
Но ссылаться на вакцину, зарегистрированную для экстренных показаний, на основании исследований первой и второй фазы, разрешения на проведение которых были оформлены задним числом, так что непонятно-- проводились они или нет, при отсутствии опубликованных результатов исследования третьей фазы, для обоснования несравненных свойств новой вакцины это, пожалуй, перебор.

Санкт-Петербург
Карма: +335.53
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Цитата: Doctor_D от 14.08.2020 18:44:14Вообще, разумеется, никакое сходство в "автомобилях", нигде не служит основанием для того, чтобы не проводить клинические исследования. Простите, даже при регистрации дженерика, имеющего не похожий, а *идентичный* состав, проводят исследования биоэквиваоентности (аналог третьей фазы).
Но ссылаться на вакцину, зарегистрированную для экстренных показаний, на основании исследований первой и второй фазы, разрешения на проведение которых были оформлены задним числом, так что непонятно-- проводились они или нет, при отсутствии опубликованных результатов исследования третьей фазы, для обоснования несравненных свойств новой вакцины это, пожалуй, перебор.
Вы уже несколько дней пишете примерно одно и тоже - вакцина не готова, караул, люди ни к коем случае не дайте себя вакцинировать...
На пути сокращения, совмещения фаз клинических испытаний идут практически все разработчики. Время работает против человечества - больных десятки миллионов, погибших сотни тысяч, ВВП стран падает на десятки процентов. Если срочно не создать вакцину, обходя в этом некоторые условности, то возможно развитие хронического процесса с трудно представляемыми последствиями в экономике, здравоохранении.
Да, ещё ответ на удалённый пост.
В обычном понятии, конечно вакцина не лекарство. Лекарство выдаётся больному человеку, а вакцинируют миллионы людей не болеющих на данный момент конкретной инфекцией. Так понятно.
По поводу возрастных ограничений, то практически все вакцины в настоящее время нацелены на применение в возрастном диапазоне 18-60 лет. Для других возрастов дозировки будут определяться в ходе следующих клинических испытаний вакцины.
De die in diem verba volant, scripta manent - изо дня в день слова исчезают, написанное остаётся

Санкт-Путинбург
Карма: +56.47
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Регистрация: 31.10.2008
Сообщений: 6,436
Читатели: 7
Цитата: зарун от 14.08.2020 18:25:17Англо-американская вакцина против Эбола - rVSV-ZEBOV хотя и получила разрешение на профилактическое применение среди населения ДРК в очаге лихорадки Эбола, но эффективность её оказалась низкой, о чём говорит высокая смертность среди вакцинированных
пациентов - более 20%. Поэтому рано петь дифирамбы по амерской вакцине.
Да дифирамбы никто и не поёт. Тоже рекомбинантная на аденовирусе, но на другом. Просто это единственная вакцина, по которой есть достоверные сведения об её массовом использовании. Наша вакцина только только прошла испытания, но её эффективность оценивалась по результатам ИФА. Как она поведёт себя при встрече вакцинированного с настоящим вирусом - пока неизвестно. На бумаге по ИФА у Мерк тоже всё было супер. Хотя защита 80% - это несравненно намного лучше, чем её отсутствие.
Карма: +18.74
Регистрация: 06.08.2008
Сообщений: 1,531
Читатели: 0
Регистрация: 06.08.2008
Сообщений: 1,531
Читатели: 0
Цитата: зарун от 14.08.2020 18:57:01Вы уже несколько дней пишете примерно одно и тоже - вакцина не готова, караул, люди ни к коем случае не дайте себя вакцинировать...Человек пишет, что 2+2=4. "Не прошло все испытания - значит еще не лекарство" вбито в подкорке на этом же уровне у любого человека связаного с медицинской темой (неважно как врач, как научный сотрудник, или как еще).
ЦитатаНа пути сокращения, совмещения фаз клинических испытаний идут практически все разработчики.Какие то сокращения есть, но испытания 3-й фазы все остальные, от "Вектора", до китайцев и западных разработчиков собираются провести.
ЦитатаВремя работает против человечества - больных десятки миллионов, погибших сотни тысяч, ВВП стран падает на десятки процентов. Если срочно не создать вакцину, обходя в этом некоторые условности, то возможно развитие хронического процесса с трудно представляемыми последствиями в экономике, здравоохранении.От непроверенного препарата могут проблемы не меньше. Начиная от побочек, и кончая ложным чуством защищенности, если выяснится что иммунитет не стойкий (поскольку само наличие антител еще не гарантирует защиту. Титр антител может быть недостаточен для иммунитета. Или достаточный что бы быть без симптомов, но оставатся заразным, что едва ли не хуже. Или куча других проблем которые никак нельзя спрогнозировать на выборке из нескольких десятков человек за пару месяцев.
Да, ещё ответ на удалённый пост.
Более того, как уже писали, создается опасный прецедент с коммерческим использованием непровенного препарата.
ЦитатаВ обычном понятии, конечно вакцина не лекарство.Имеется ввиду профессиональное и юридическое понимание. Лекарственный препарат должен обладать доказнной эффективностью, и информация о том, какой риск несет применение. Это делается не просто так, это в том числе что бы мешать БАДам, травным настоям и пр. мимикрировать под лекаства.

Санкт-Петербург
Карма: +335.53
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Регистрация: 23.08.2012
Сообщений: 14,054
Читатели: 7
Цитата: Doctor_D от 14.08.2020 19:08:26Да, вакцина не готова. Её эффективность и безопасность не доказана. Исследование первой фазы на 38 добровольцах-- это недостаточно. Прививаться этим- русская рулетка. И обстоятельства никак не оправдывают примитивно го шулерства. Обратите внимание, что все, даже китайцы, проводят разработку по правилам. Хотя имеют вакцины в той же, если не больше, степени готовности.
И да, я против того, чтобы данные по безопасности и эффективности этой вакцины, ради престижа и барышей от экспорта, собирались путем экспериментов над нашим населением. У меня не так много принципов, но "не навреди" это один из них. Так уж научили, простите.
И, ещё, не хочется возвращаться во времена до Нюрнбергского Кодекса. Всё же, для него потребовал одноимённый трибунал и все, что ему предшествовало. И самое обидное, что тянут туда не недобитые фашисты...
А где вы видели установленные стандарты по количеству испытуемых? Мне встречалось требование по объёму клинических испытаний только у FDA - минимум 3000 человек на все фазы клинических испытаний вакцин. Российская вакцина будет испытана на большем количестве пациентов во всех трёх фазах клинических испытаниях.
Почему вас так беспокоит, что как будто-то бы отсутствует безопасность вакцины? В общей сложности испытания прошли более 70 человек. Сведений о тяжёлых осложнений и, тем более, летальных исходов сразу после вакцинации и в период 1 - 2 месяца после них нет, то нет сомнения, что вакцина безопасна. Более того безопасность препарата будет продолжается изучаться и в следующих фазах испытания.
Все участники мировой гонки по созданию вакцины против SARS-CoV-2 не укладываются в стандартные сроки. Более того до настоящего времени наименьший срок до промышленного производства был у вакцины против инфекционного паротита - 4 года. Но даже этот короткий срок от начала работ до начала массовой иммунизации не может быть приемлем к COVID-19.
De die in diem verba volant, scripta manent - изо дня в день слова исчезают, написанное остаётся

Москва
51 год
Карма: +344.16
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Регистрация: 21.02.2008
Сообщений: 9,520
Читатели: 7
Цитата: зарун от 14.08.2020 21:05:02А где вы видели установленные стандарты по количеству испытуемых? Мне встречалось требование по объёму клинических испытаний только у FDA - минимум 3000 человек на все фазы клинических испытаний вакцин. Российская вакцина будет испытана на большем количестве пациентов во всех трёх фазах клинических испытаниях.
Почему вас так беспокоит, что как будто-то бы отсутствует безопасность вакцины? В общей сложности испытания прошли более 70 человек. Сведений о тяжёлых осложнений и, тем более, летальных исходов сразу после вакцинации и в период 1 - 2 месяца после них нет, то нет сомнения, что вакцина безопасна. Более того безопасность препарата будет продолжается изучаться и в следующих фазах испытания.
Все участники мировой гонки по созданию вакцины против SARS-CoV-2 не укладываются в стандартные сроки. Более того до настоящего времени наименьший срок до промышленного производства был у вакцины против инфекционного паротита - 4 года. Но даже этот короткий срок от начала работ до начала массовой иммунизации не может быть приемлем к COVID-19.
Слушайте, вы или прикидыапетесь, что не понимаете, либо, сознательно игнорирует факты. Я думаю, что второе. В любом случае, не вижу смысла повторять очевидное по третьему разу.
Если вы хотите прививаться этой вакциной и прививать ей своих близких-- ваше право. Каждый волен делать с собой что хочет.
Я- не буду и родным не дам. И постараюсь дать информацию для принятия информированного решения максимальном числу людей. Профессиональный долг, однако.
Дополню по требованиям американского регулятора FDA:
ЦитатаКлиническая разработка должна быть стандартной для препарата, направленного на профилактическое применение. Возможно использование адаптивных или бесшовных дизайнов, которые могут позволить ускорить принятие решений. Поздние фазы исследований могут потребовать включения многих тысяч пациентов. Во все клинические исследования целесообразно включать различные субпопуляции, которые отражали бы фактическую демографическую и морбидную структуру населения. Исследования поздних фаз должны быть рандомизированными, двойными слепыми и плацебо-контролируемыми, причем рандомизация 1:1 обычно является наиболее эффективным подходом для подтверждения эффективности. Возможно изучение нескольких вакцин в одном исследования по отношению к одной и той же группе плацебо.
Первичной конечной точкой может быть лабораторно подтвержденное заболевание COVID-19 или лабораторно подтвержденная SARS-CoV-2-инфекция. Сформулированы требования к обязательным вторичным, среди которых тяжелое течение COVID-19.
Статистические критерии эффективности:оценка первичной конечной точки эффективности в плацебо-контролируемом клиническом исследовании должна составлять по меньшей мере 50%, а статистическим критерием успеха должна быть ситуация, когда нижняя граница соответствующим образом скорректированного по альфа доверительного интервала вокруг оценки первичной конечной точки эффективности >30 %. Такой же критерий следует использовать для всех промежуточных анализов. В случае не меньшей эффективности, если к моменту разработки вакцины будет существовать другая эффективная вакцина, критерием успеха должна быть ситуация, когда нижняя граница соответствующим образом скорректированного по альфа доверительного интервала вокруг оценки первичной конечной точки относительной эффективности > –10 %.
Предрегистрационная база безопасностидолжна состоять из не менее чем 3000 участников.
...
Доклинические свойства вакцины должны быть исчерпывающим образом охарактеризованы, особенно в случае новых вакцинных форматов, доселе не получивших широкого применения. Опорные (definitive) доклинические исследования безопасности должны быть проведены в соответствии с GLP, включая исследования онтогенетической и репродуктивной токсичности (DART), требуемые перед включением в исследования женщин с детородным потенциалом. Обязательны исследования биораспределения в отношении новых конструкций, а также установление характеристик иммунного ответа на животных (гуморального и клеточного), включая оценку потенциала вакцин-ассоциированного усугубления поражения дыхательной системы.
Отредактировано: Doctor_D - 14 авг 2020 21:44:33
Карма: +219.74
Регистрация: 12.02.2009
Сообщений: 6,363
Читатели: 3
Регистрация: 12.02.2009
Сообщений: 6,363
Читатели: 3
Цитата: basilevs от 14.08.2020 14:26:00Есть мощности под инактивированные вакцины - например, у "гриппозников". То есть сделав инактивированную вакцину, которую можно выпускать на "гриппозных" мощностях с минимальными их переделками - можно реально остановить эпидемию.
А разве "гриппозные" технологии вообще подойдут? Там же вирус нарабатывают в зародышах оплодотворённых куриных яиц, а SARS-CoV-2 в них вроде не размножается?
Сейчас на ветке:
20,
Модераторов: 0,
Пользователей: 0,
Гостей: 2,
Ботов: 18
