Были или нет американцы на Луне?
12,721,217
105,808
|
|
sharp89 ( Слушатель ) |
| 18 ноя 2019 23:54:52 |
Коноваловщина
новая дискуссия Дискуссия 6.160Цитата: михайло потапыч от 18.11.2019 22:52:25Эти застывшие куклы на крупном песке.
Ох уж эти коноваловские неподвижные куклы


Одного примера тут более чем достаточно, чтобы показать, во что Коновалов ставит своего читателя.
Ну что, включится скептицизм, или нет?

ОТВЕТЫ (1094)
|
|
South ( Слушатель ) |
| 19 ноя 2019 00:05:40 |
Цитата: sharp89 от 18.11.2019 23:54:52
Ну и видно же что кукла имеет одну и ту же позу меняется только точка съемки.
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 10:34:26 |
Цитата: South от 19.11.2019 00:05:40
А как насчет глаза разуть?


Меняется положение ноги относительно камней на грунте, меняется форма тени от астронавта, меняются тени на PLSS (то есть изменился наклон PLSS относительно направления на источник света). Таким образом "кукла" меняет свою позу, а значит это и не кукла вовсе.
|
|
Будимир ( Слушатель ) |
| 19 ноя 2019 10:54:47 |
Цитата: sharp89 от 19.11.2019 10:34:26
У меня нескромный вопрос к тем, кто пользовался плёночными аппаратами, особенно хасселями и его копиями – какое минимальное количество времени на перезарядку плёнки для повторного кадра и сколько за это время должен был пройти лунотопталец?
Вот здесь есть более наглядный ряд из трёх фото:

|
|
Громозека ( Слушатель ) |
| 19 ноя 2019 10:58:09 |
Цитата: Будимир от 19.11.2019 10:54:47
Надо посмотреть конструкцию фотоаппарата. Как минимум нужно время на перемотку пленки на следующий кадр, если там не было электропривода для перемотки.
|
|
Будимир ( Слушатель ) |
| 19 ноя 2019 11:00:15 |
Цитата: Громозека от 19.11.2019 10:58:09
Если был электропривод, то инженерам нужно было решать проблему искр в их кислородной атмосфере.
Если не было, то времени для перемотки нужно прилично и сдвиг на пару см за этот промежуток смешон. Куда ни кинь, всюду клин.



|
|
Alexxey ( Слушатель ) |
| 19 ноя 2019 12:17:35 |
Цитата: Громозека от 19.11.2019 10:58:09
А чего бы Вам было не поинтересоваться сначала конструкцией фотоаппарата и высказать нечто осмысленное, вместо того чтобы засорять ветку бессмысленным флудом?
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:14:37 |
Цитата: Будимир от 19.11.2019 10:54:47
А "лунотопталец" обязан непрерывно ходить, чтобы вы чего-то не заподозрили?
 Он там (в отличие от вас), делом занят.
Он там (в отличие от вас), делом занят.
|
|
Громозека ( Слушатель ) |
| 19 ноя 2019 11:15:05 |
Цитата: Будимир от 19.11.2019 10:54:47
У меня вот что получилось в авто тоном:

На паре фото идентичное расположение космонавта, на одном (первое фото) опять чуть сместился ракурс, поэтому опять можно выдать за движуху куклы.
Либо космонавт замер и позирует, либо серийное фото, либо куклы. Серийное фото могло быть только при автоматической перемотке.
|
|
photo_vlad ( Слушатель ) |
| 19 ноя 2019 12:44:45 |
Цитата: Будимир от 19.11.2019 10:54:47
У Хассельблада с автоматической протяжкой плёнки очень неспешный механизм.
А ещё нужно повторно на спуск затвора в толстой нечувствительной перчатке нажать.
Не менее трёх секунд должно пройти между экспозицией кадров.
|
|
Alexxey ( Слушатель ) |
| 19 ноя 2019 13:08:35 |
https://www.ibiblio.org/apollo…973-06.pdf
"The HEC motor drive provides automatic recocking of the lens shutter and film advancement after each exposure. The exposure is initiated by depressing the operate button on the camera front. Releasing the operate button activates the camera motor which automatically stops at the completion of the drive functions (approximately 1.0 second run duration)"
"Моторный привод HEC (Hasselblad Electric Camera) обеспечивает взведение затвора и перемотку пленки после каждой экспозиции. Экспозиция инициируется нажатием кнопки управления на передней панели камеры. Отпускание кнопки управления активирует мотор камеры, который автоматически останавливается по завершении взведения затвора и перемотки плёнки (длительность работы около 1,0 секунды)"
|
|
Удаленный пользователь |
| 21 ноя 2019 20:25:21 |
Цитата: Alexxey от 21.11.2019 17:29:09
Вы бредите? Хорошо, приведите цифровые значения для давлений воды и воздуха на границе их раздела, в сосуде, наполовину заполненном водой при нормальных условиях, и герметично закрытом крышкой.
Цитатаим соответствуют РАЗНЫЕ точки на фазовой диаграмме, за счёт наличия других атмосферных газов.
Какие разные точки? Мы говорим о нормальном атмосферном давлении. Как Вам помогут "другие газы", если критическое давление у них гораздо ниже, чем у пара, а, поскольку они в воздухе находятся в газообразном состоянии при t выше критической (кроме СО2), значит и их "флюид" по сути ничем от пара/газа не отличается.
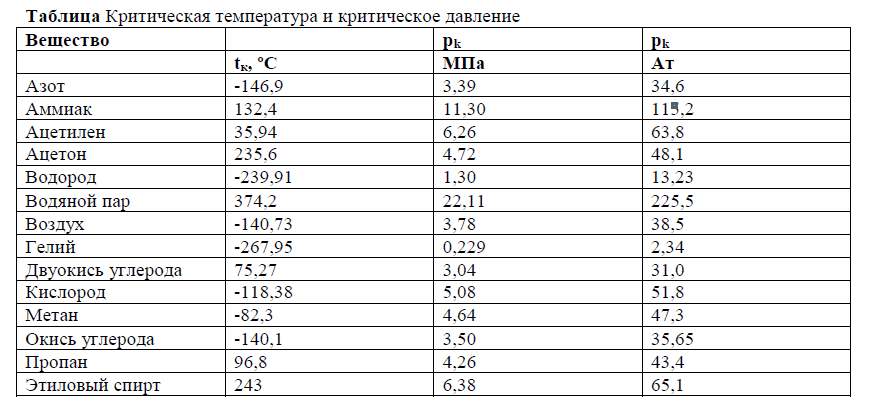
ЦитатаПри отсутствии других веществ, жидкость и пар сосуществуют только на линии насыщения (при установившемся динамическом равновесии испарения/конденсации), в любых других условиях (других точках фазовой диаграммы) — либо только жидкость, либо только пар
Понятно, у Вас плавки после купания не сохнут.
 Не бывает так, чтобы в замкнутом объёме сосуществовали области с разным давлением. Продемонстрируйте, пожалуйста, причудливые формы шарика, надутого слоями воздух-гелий-кислород, демонстрирующие разницу давлений по слоям. А я поудивляюсь вместе с Вами. Или можете накачать, например, лодку гелием, а потом открыть клапан. Посмотрим вместе, останется ли давление в лодке на прежнем уровне.
Не бывает так, чтобы в замкнутом объёме сосуществовали области с разным давлением. Продемонстрируйте, пожалуйста, причудливые формы шарика, надутого слоями воздух-гелий-кислород, демонстрирующие разницу давлений по слоям. А я поудивляюсь вместе с Вами. Или можете накачать, например, лодку гелием, а потом открыть клапан. Посмотрим вместе, останется ли давление в лодке на прежнем уровне.Ваш подход к подсчету давления путем процентного отношения количества пара в воздухе к общему объёму в данном случае сродни подсчету температуры молекулы кипящей воды путём деления температуры кипения на количество молекул.
Вода при изменении давления с нормального до 25МПа и температуре 20 градусов изменит свой объём на 1,1 процента и перестанет испаряться. В остальном объёме как был газ, так он и останется. Неужели это так сложно понять?
|
|
South ( Слушатель ) |
| 19 ноя 2019 11:12:38 |
Цитата: sharp89 от 19.11.2019 10:34:26
Да ну
 ?
?Вот вам копилка:



.
.
Меняется местоположение уха относительно ножниц
меняются тени на на морде от пятачка, то есть есть наклон относительно направления на источник света.
Таким образом "копилка" меняет свою позу, а значит это и не копилка вовсе.
.
.

|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:17:22 |
Цитата: South от 19.11.2019 11:12:38
Как обычно троллизм у вас получается слишком толсто.
Для утверждения, что вместо астронавта, нужны какие-то основания. Коновалов в качестве такого "обоснования" использовал неподвижность, однако теперь мы наблюдаем, что "неподвижность" ложная. Что остается - это куклы, потому что опровергам так хочется?

|
|
South ( Слушатель ) |
| 19 ноя 2019 11:29:38 |
Цитата: sharp89 от 19.11.2019 11:17:22
Вы как обычно ничего не поняли, это не троллизм, а пример вашей тупости, смотреть изменения надо не относительно поверхности а изменения относительно частей тела самой куклы, а они на фото не меняются( снять так живого человека очень сложно даже если он позирует а вы снимаете на скоростной современный аппарат, а уж случайно получить одну и ту же позу человека в работе да еще соседними кадрами практически не возможно. А так да относительно поверхности изменились, я тоже свинью повернул и она тоже поменяла свое положение относительно освещения, стола и предметов на нем.
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:38:15 |
Цитата: South от 19.11.2019 11:29:38
Наклон туловища к поверхности поменялся.
Хотя я знаю что вы на это ответите - кукловоды не только переставляли куклу, но и слегка гнули ей позу

|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:51:33 |
Цитата: Громозека от 19.11.2019 11:50:08
А в видеозаписях лунных трансляций тоже кукольный мультфильм?

|
|
South ( Слушатель ) |
| 19 ноя 2019 12:00:53 |
Цитата: sharp89 от 19.11.2019 11:38:15
Мне свинью набок положить, что бы до вас дошло что нужно измерять не всю фигуру относительно поверхности и света, а отдельные ее части относительно других частей тела частей тела.
|
|
South ( Слушатель ) |
| 19 ноя 2019 13:26:58 |
Цитата: sharp89 от 19.11.2019 12:06:26
Пожалуйста:


Правый астронахт вырезан из другого фото, в красном обводе строго масштабированная версия наложенная на второе фото. По параллельности линий обвода прекрасно видно что угол тела у них один и тот же, а если есть легкие отклонения то они вызваны смещением точки фотографирования.
|
|
photo_vlad ( Слушатель ) |
| 19 ноя 2019 13:30:08 |
Цитата: South от 19.11.2019 13:26:58
1. Положение фигуры
2. Складки на лунных штанах
3. И тени от фигур на обеих фото одинаковы.
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 13:40:35 |
Было показано на предыдущей гифке, что разные и тени от фигур, и тени на самом астронавте (в особенности на PLSS).

Так что не плюхайтесь уж так с разбегу в лужу, Владимир. Кстати, как вас там по настоящей фамилии?
|
|
South ( Слушатель ) |
| 19 ноя 2019 13:45:49 |
Цитата: sharp89 от 19.11.2019 13:40:35
Вам было показаны разные тени от фигуры хрюшки и тенина самой тушке но вас это почему то не впечатляет.
|
|
михайло потапыч ( Слушатель ) |
| 19 ноя 2019 07:14:50 |
Цитата: sharp89 от 18.11.2019 23:54:52
На этих фото тоже откажетесь куклу увидеть?
Взято из статьи Леонида Коновалова Использование кукол в миссиях Аполлон
|
|
Technik ( Слушатель ) |
| 19 ноя 2019 07:34:39 |
"Куклы на фотографиях всегда обездвижены" - из этой статьи...
Sharp прав насчет того, во что Коновалов ставит своего читателя. И вас тоже, милейший Потапыч.
Вы бы хоть на секунду задумались бы - а что, на ФОТОГРАФИЯХ "куклы" должны ходить и двигаться, как на видео или кинофрагментах?
Интересно, приверженность к конспирологии оставляет какой-то след на внешности? Было бы любопытно посмотреть на вас, Потапыч - в этом плане вы отличный образец для соответствующего исследования (и привет вам от голографических Боингов...
 ).
).
|
|
Дмитрий_A ( Слушатель ) |
| 19 ноя 2019 08:05:19 |
Цитата: Technik от 19.11.2019 07:34:39
Не подскажете, как в Хасселе удалось решить проблему искрения коллекторно-щеточного узла в кислородной атмосфере? При первом же включении Хасселя должно было рвануть, ну, или как минимум пожар. Может так и сгорел один их экипаж?
|
|
Будимир ( Слушатель ) |
| 19 ноя 2019 08:12:38 |
Цитата: Дмитрий_A от 19.11.2019 08:05:19
Про хассель хз, но про видеокамеру действительно было бы интересно) А то опять советские лопухи спецкамеру разрабатывали на герконах и с магнитной муфтой, делать, видимо, нечего было.



|
|
Technik ( Слушатель ) |
| 19 ноя 2019 08:40:40 |
Цитата: Дмитрий_A от 19.11.2019 08:05:19
Точного ответа на этот вопрос у меня нет, но полагаю, что и эта проблема, как и миллион прочих, в ходе успешного выполнения программы Аполлон была успешно решена. Тем более что после пожара на А-1, как сообщает Вики, НАСА выдвинула дополнительные требования по безопасности электрооборудования.
Какие - ну поищите, в конце концов, сами. Всякую каку вы, уважаемые опроверги, выкапываете умело и с удовольствием - ну так примените вашу квалификацию и для поиска нормальной информации.
|
|
Дмитрий_A ( Слушатель ) |
| 19 ноя 2019 10:07:46 |
Цитата: Technik от 19.11.2019 08:40:40
В принципе такой ответ был вполне ожидаем, ибо эта проблема в Хасселях не была решена от слова "совсем".
|
|
Удаленный пользователь |
| 19 ноя 2019 10:28:05 |
Цитата: Technik от 19.11.2019 08:40:40
Добрый день всем.
Уважаемый Техник.
Не могли бы Вы объяснить, каким образом двигатель посадочной ступени дал приращение скорости при выходе на траекторию возврата всей сборки АП13 при 2 раза меньшей мощности? Ведь время работы двигателя ПС должно увеличиться в два раза. Правильно?
Запас топлива на ПС ограничен. БЦВМ не предназначена для ввода программы разгона всей сборки. Управление карданом подвеса двигателя ПС как осуществлялось? Время работы они по наручным часам считали :о))))
Смотрим табличку ниже и сравниваем.
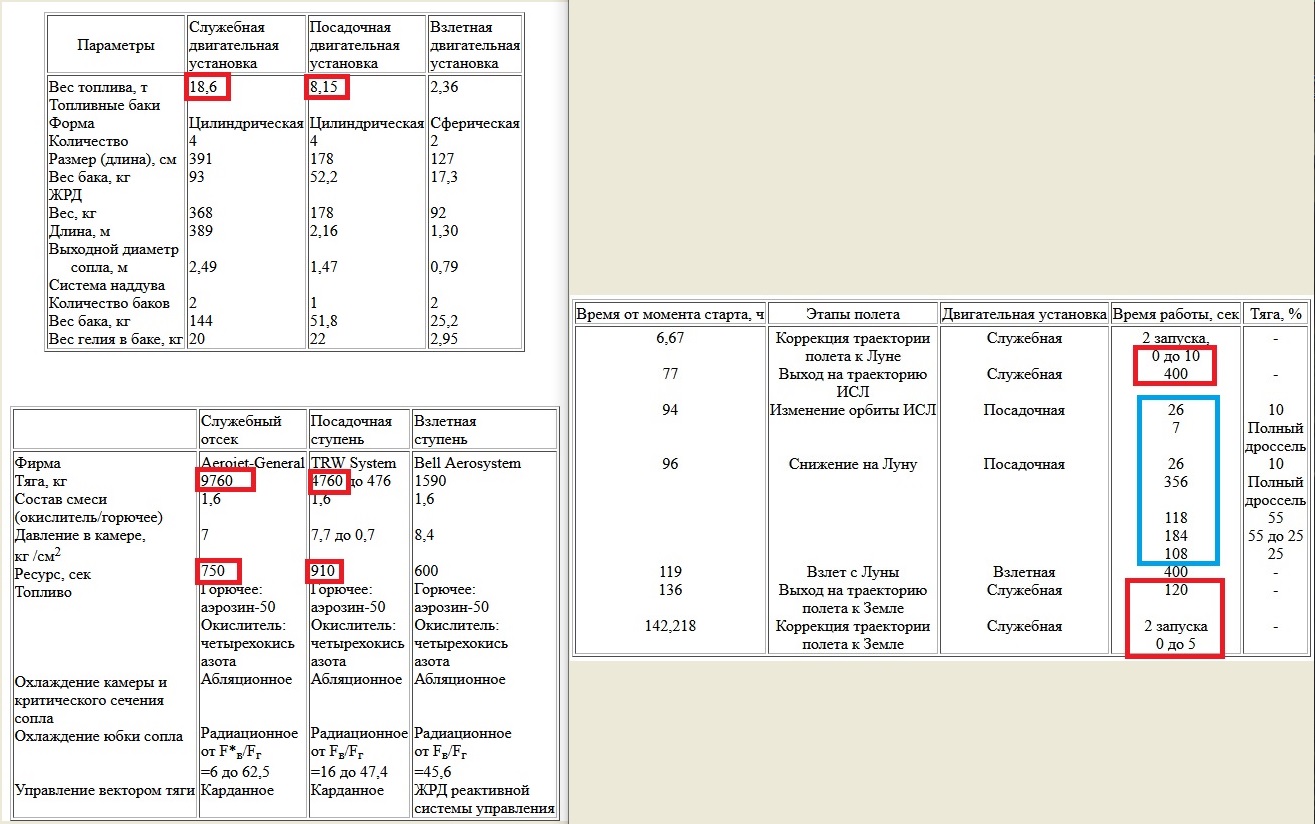
С уважением
|
|
Technik ( Слушатель ) |
| 19 ноя 2019 11:45:07 |
Цитата: Протеин от 19.11.2019 10:28:05
Цитата: Протеин от 19.11.2019 10:28:05
У меня сейчас другая тема в работе, отвлекаться более не намерен. Вот выложу соответствующий текст - тогда может быть когда-нибудь. И то вряд ли, нам с вами следует отработать общий сценарий аферы - несколько набросков к которому вы довольно-таки давно разместили.
А чтобы вам было над чем НЕ думать, а просто заклеймить злобную НАСУ как фальсификаторов всего и вся - подкину вам материальчик для этого (если уже его вам давал, не взыщите, в пылу борений с вами, опровергами, последний разум теряется...)
https://glav.su/blog/34420/1266067/
https://glav.su/foru…age4695772
|
|
Громозека ( Слушатель ) |
| 19 ноя 2019 10:55:40 |
Цитата: sharp89 от 19.11.2019 10:42:08
Sorry, еще не дошел. Говоря "по чесноку", фото не очень убедительно доказывает движение космонавта.
Если бы ракурс не менялся, то "адназначна" можно было бы констатировать, что движуха была.
Надо исходники смотреть. На этих гиффках не все так однозначно.
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:12:40 |
Цитата: Громозека от 19.11.2019 10:55:40
Это кадры 11436 и 11437. Это соседние кадры панорамы, то есть фотограф только поворачивался, но не переходил с места на место:


|
|
Громозека ( Слушатель ) |
| 19 ноя 2019 11:25:51 |
Цитата: sharp89 от 19.11.2019 11:12:40
Как быстро космонавт мог перемотать пленку на следующий кадр? Это ответ на Ваш вопрос.
Если на это уходит около 5 сек., то прав Коновалов. Только он не учел, что мультипликаторы не зря свой хлеб едят. Они с каждым кадром в мультике, чуть-чуть сдвигают фигуры для избежания статичных сцен.
|
|
Sinbad ( Слушатель ) |
| 19 ноя 2019 11:34:28 |
Цитата: Громозека от 19.11.2019 11:25:51
У Коновалова есть об этом: "Пленочный фотоаппарат "Хассельблад" снимает не так быстро, как современные цифровые фотоаппараты (в определённом режиме цифровой фотоаппарат может снимать по несколько кадров в секунду). А как снимает "Хассельблад"? После нажатия спусковой кнопки в фотоаппарате вдоль плёнки пробегает световая щель между двумя движущимися шторками затвора, после этого включается мотор на перемотку пленки на следующий кадр. Это длится около двух секунд."
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:35:26 |
Цитата: Громозека от 19.11.2019 11:25:51
"electric-motor-driven mechanism advances the film" https://history.nasa.gov/afj/ap16fj/02photoequip.html
То есть, перемотка с электроприводом. Точную скорострельность я так сходу не скажу, но это в любом случае единицы секунд. Где-то есть видео астронавта, снимающего панораму (позже попытаюсь найти), там видно, что паузы между соседними кадрами очень маленькие.
ЦитатаОни с каждым кадром в мультике, чуть-чуть сдвигают фигуры для избежания статичных сцен.
Так где доказательства кукольности? Правильно понимаю, доказательств нет, просто с подачи Коновалова вам захотелось думать что это куклы?

|
|
Громозека ( Слушатель ) |
| 19 ноя 2019 11:46:44 |
Цитата: sharp89 от 19.11.2019 11:35:26
Электропривод ставит под сомнение работу в чистом кислороде. Они ведь и внутри корабля снимали по легенде?
Цитата: sharp89 от 19.11.2019 11:35:26
Я высказал по данному вопросу свою версию, причем несколько.
Но можно уверенно заявить, что незначительные движения кукол тоже можно подделать, если мультипликаторы опытные.
Либо космонавт позировал, что не исключает павильонной съемки.
Либо это было на Луне и фотоаппарат продемонстрировал великолепные результаты работы в вакууме и среде чистого кислорода.
|
|
sharp89 ( Слушатель ) |
| 19 ноя 2019 11:50:29 |
Вообще ни разу не ставит.Цитата: Громозека от 19.11.2019 11:46:44
ЦитатаЛибо это было на ЛунеДа, это наиболее вероятный вариант.